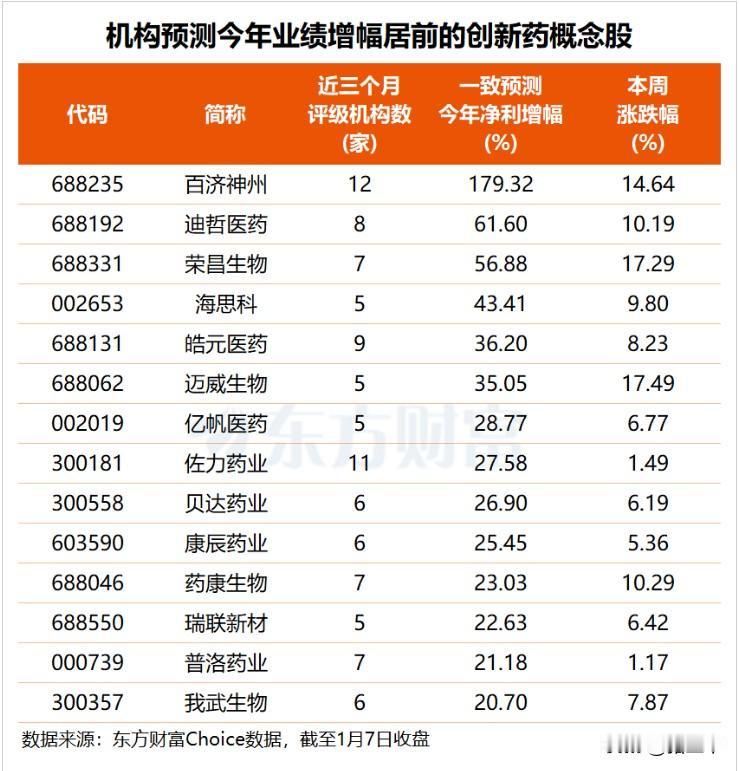
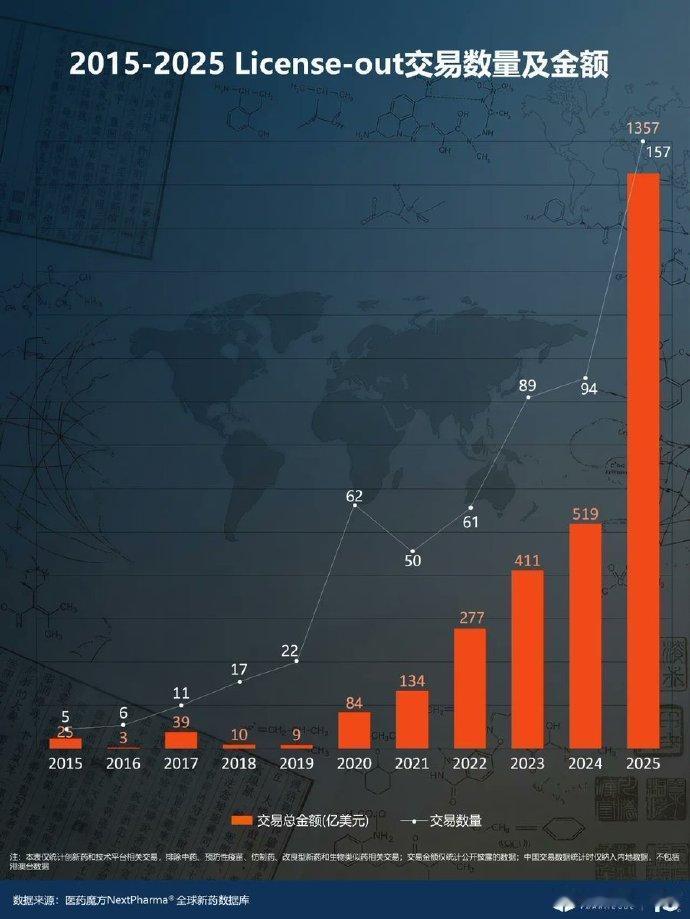
13日,商业航天板块跌幅居前。其中顺灏股份、中国卫通等多股跌停。不过,调整良久的创新药板块开始重新崛起。
截至收盘,荣昌生物、泓博医药、博济医药、康乐卫士等个股涨停;港股方面,基石药业、启明医疗、荣昌生物、石药集团等公司表现亮眼。
CXO企业的全球化服务能力,是中国创新药出海的重要支撑。受上述消息提振,诺思格、泰格医药、药明康德、药明巨诺、康龙化成等CXO公司今日股价亦表现不凡。
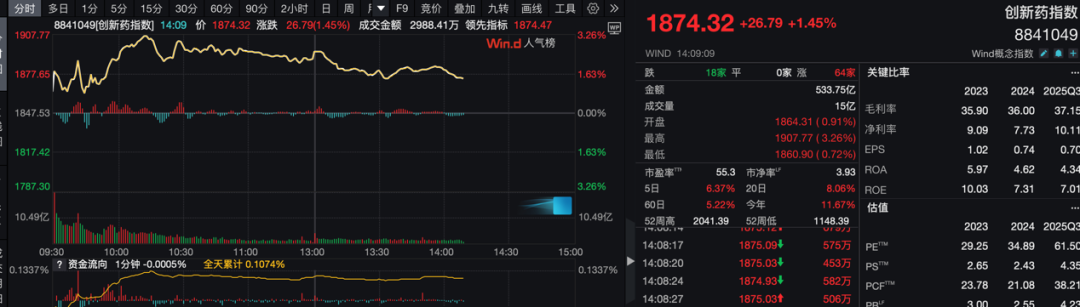
消息面上,第44届摩根大通医疗健康大会(JPM2026)于1月12日至15日在美国旧金山召开,此次会议聚焦生物技术、生物制药、AI+医药等六大领域。作为全球生物医药行业的“春晚”,每年1月举办的JPM大会是全球医药行业最重要的投资与交易窗口之一,可一睹全球医药生物产业发展的最新动态。
多家公司将公布研发进展
2025年以来,国内创新药企发力海外市场各显身手、大放异彩。中国创新药正完成从“快速追随者”到“体系创新者”的跃迁。
此次JPM大会是众多生物医药公司发布最新临床研究成果的重要平台。约24家国内创新药企将在会议上展示优异临床数据,彰显中国药企国际竞争力。
其中,主会场演讲企业包含7家,包括药明康德、药明生物、药明合联3家CXO公司,以及百济神州、再鼎医药、亚盛医药、传奇生物4家创新药公司。
例如,复宏汉霖将围绕公司全球化2.0阶段的发展路径、创新管线布局及中长期战略规划,分享公司最新进展与未来蓝图。目前,复宏汉霖产品覆盖肿瘤、自身免疫疾病、眼科疾病等领域,已在全球获批上市10款产品。公司已获批上市的汉斯状(斯鲁利单抗)是全球首个获批一线治疗小细胞肺癌的抗PD-1单抗;公司自主研发的汉曲优(曲妥珠单抗)系中美欧三地获批单抗生物类似药;汉利康(利妥昔单抗)则为国内首个生物类似药。
百济神州将会介绍CDK4等核心产品进展。公司目前拥有三款已商业化产品。其中,百悦泽(泽布替尼)是全球获批适应症最广泛的BTK抑制剂,已在美国获批用于治疗慢性淋巴细胞白血病、套细胞淋巴瘤、华氏巨球蛋白血症、边缘区淋巴瘤、滤泡性淋巴瘤等多项适应症。百泽安(替雷利珠单抗)是由百济神州自主研发、结构优化的创新型PD-(L)1抑制剂,已获批鼻咽癌、食管癌、胃癌、肝癌、尿路上皮癌等14项适应症,其中13项已纳入医保,是国内获批适应症覆盖最广泛、医保覆盖适应症数量最多的PD-1产品。
日前,百济神州新型BCL2抑制剂百悦达®(索托克拉片)获国家药监局附条件批准上市,是中国首款且唯一获批用于治疗套细胞淋巴瘤的BCL2抑制剂。
此外,亚盛医药将会介绍公司细胞凋亡管线进展。公司已建立丰富的创新药产品管线,包括抑制Bcl-2和MDM2-p53等细胞凋亡通路关键蛋白的抑制剂;新一代针对癌症治疗中出现的激酶突变体的抑制剂等。其核心品种耐立克是中国首个获批上市的第三代BCR-ABL抑制剂,且获批适应症均被成功纳入国家医保药品目录,公司另一重磅品种利生妥是中国首个获批上市的国产原创Bcl-2抑制剂,已获批用于既往经过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的成人慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)患者。目前,亚盛医药正在开展利生妥®四项全球注册III期临床研究。
除此之外,恒瑞医药、百利天恒、三生制药、荣昌生物等17家国产创新药企也将亮相亚太专场。
三生制药拥有40余种上市产品,覆盖肾科、肿瘤科、自身免疫性疾病、眼科及皮肤科等多种治疗领域。根据Insight数据库,截至目前,三生制药已有5款新药处于上市审评阶段,包括IL-17A创新单抗SSGJ-608、IL-1β单抗SSGJ-613、贝伐珠单抗眼内注射溶液601A等。
2025年,三生制药共达成了2笔BD交易,一笔是授予辉瑞PD-1/VEGF双抗SSGJ-707全球开发和商业化权利;另一笔是获得了映恩生物HER2ADC药物DB-1303多个适应症在国内的商业化合作权利。
1月6日,百利天恒自研新药iza-bren(BL-B01D1)的新增适应症已被国家药监局药品审评中心(CDE)纳入优先审评程序,适应症为既往经PD-1/PD-L1单抗联合含铂化疗治疗失败的复发性或转移性食管鳞癌。这已经是iza-bren除了晚期鼻咽癌之外,第二项被纳入优先审评程序的适应症。
Iza-bren是全球首创(First-in-class)、新概念(Newconcept)且唯一进入III期临床阶段的EGFR×HER3双抗ADC,iza-bren正在中国和美国进行40余项针对多种肿瘤类型的临床试验。截至目前,iza-bren已获得CDE的7项突破性疗法认定,和美国食品药品管理局(FDA)的1项突破性疗法认定。
已达成5项BD交易
按以往来看,JPM大会召开期间,全球创新药领域的BD(商务拓展)交易和收购动作均表现活跃。
日前,已有重磅BD交易揭晓:1月12日晚间,荣昌生物宣布,与跨国药企艾伯维就荣昌生物自主研发的新型靶向PD-1/VEGF双特异性抗体药物RC148签署独家授权许可协议。
根据协议,艾伯维将获得RC148在大中华区以外地区的独家开发、生产和商业化权利。荣昌生物将收到一笔6.5亿美元的首付款,并有资格获得最高达49.5亿美元的开发、监管和商业化里程碑付款,以及在大中华区以外地区净销售额的两位数分级特许权使用费。
目前,荣昌生物已有泰它西普、维迪西妥单抗2款产品获批上市,同时还有1款针对眼部新生血管性疾病的VEGF/FGF双靶标融合蛋白药物RC28-E正处于上市审评阶段。此外,荣昌生物还有PD-1/VEGF双抗、MSLNADC等重磅产品进入临床阶段。

据统计,1月以来,国内创新药已落地5项对外授权合作,涵盖小分子抑制剂、单抗、双抗、ADC和RDC,展现出中国在各个技术领域的全球领先布局。
除荣昌生物之外,1月9日,宜联生物宣布已与罗氏就YL201项目达成一项新的独家许可协议。宜联生物将获得5.7亿美元首付款及近期里程碑付款,并有权获得额外的开发、注册和商业化里程碑付款,以及YL201在海外获批上市后基于净销售额的分级特许权使用费。在中国,YL201已进入用于小细胞肺癌和鼻咽癌适应症的两项III期注册性临床试验阶段。
同日,1月9日,海思科与AirNexis就HSK39004项目签订许可协议交易额最高超10亿美元。HSK39004是一种PDE3/4的双重抑制剂,用于慢性阻塞性肺病(COPD)辅助维持治疗,当前在中国进行Ⅱ期临床试验。
此外,1月12日,中晟全肽宣布,已与诺华就放射性配体疗法(RadioligandTherapies,RLTs)领域一款未披露的多肽类资产达成全球授权与合作协议。根据协议,诺华获得该资产的全球独家授权,并将主导后续所有研发及商业化相关工作。
赛神医药亦与诺华达成合作,共同开发用于治疗阿尔茨海默病的潜在抗体疗法。根据协议条款,赛诺神经将获得1.65亿美元的预付款,后续还可依据药物研发、监管审批及产品销售等关键里程碑节点,获取最高15亿美元的里程碑付款。